ভূমিকা (Introduction): রসায়ন হলো বিজ্ঞানের এমন একটি শাখা যা পদার্থের গঠন, প্রকৃতি এবং বিভিন্ন বস্তুর ভৌত ও রাসায়নিক ধর্ম নিয়ে আলোচনা করে। ফরাসি রসায়নবিদ ল্যাভয়জিয়ার (1743–1794) কে আধুনিক রসায়নের জনক বলা হয়।
পদার্থ ও তার প্রকৃতি
যে কোনো বস্তু যা স্থান দখল করে, ভর রয়েছে এবং আমাদের এক বা একাধিক ইন্দ্রিয় দ্বারা অনুভব করা যায়, তাকে পদার্থ বলা হয়।
প্রাচীন ভারতীয় দার্শনিকরা পদার্থকে পাঁচটি মৌলিক উপাদানে ভাগ করেছিলেন, যাকে বলা হতো পঞ্চ তত্ত্ব। এগুলি হলো মাটি, আগুন, আকাশ, জল ও বায়ু। তাদের মতে জীবিত বা জড় সবকিছুই এই পাঁচ উপাদানে গঠিত। প্রাচীন গ্রিক দার্শনিকরাও একই ধরনের ধারণা দিয়েছিলেন।
ভারতীয় ঋষি মহর্ষি কানাদ প্রথম বলেন যে সমস্ত পদার্থ খুব ক্ষুদ্র কণিকা দ্বারা গঠিত। তিনি এই কণিকাগুলিকে পরমাণু নামে অভিহিত করেন। গ্রিক চিন্তাবিদ ডেমোক্রিটাস এই ক্ষুদ্র কণিকাগুলিকে Atom বলেন, যার অর্থ অবিভাজ্য। অর্থাৎ পদার্থ ক্ষুদ্র কণিকা পরমাণু দ্বারা গঠিত।
🧪 পদার্থের শ্রেণিবিভাগ (Classification of Matter)
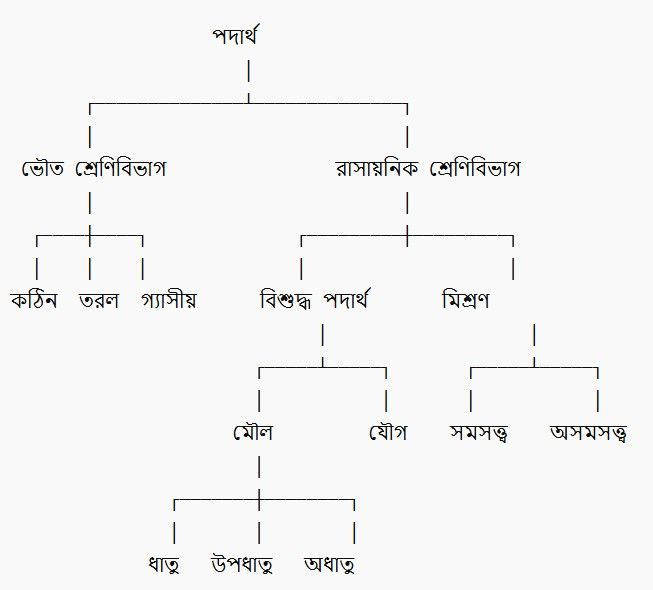
- কঠিন অবস্থা (Solid State): কঠিনের নির্দিষ্ট আকার ও নির্দিষ্ট আয়তন থাকে। তাই চাপ প্রয়োগ করলেও সহজে সংকুচিত হয় না। সাধারণত কঠিন পদার্থ শক্ত ও দৃঢ়। উদাহরণ ধাতু, কাঠ, ইট, তামা।
- তরল অবস্থা (Liquid State): তরলের নির্দিষ্ট আয়তন থাকে, কিন্তু নির্দিষ্ট আকার নেই। এটি পাত্রের আকার ধারণ করে। উদাহরণ জল, দুধ, তেল, অ্যালকোহল।
- গ্যাসীয় অবস্থা (Gaseous State): গ্যাসের নির্দিষ্ট আকার বা আয়তন কোনোটিই নেই। চাপ প্রয়োগ করলে সহজে সংকুচিত হয় এবং পাত্রের সম্পূর্ণ স্থান দখল করে। উদাহরণ বায়ু, অক্সিজেন, নাইট্রোজেন, অ্যামোনিয়া, কার্বন ডাই অক্সাইড।
- প্লাজমা অবস্থা (Plasma State): পদার্থের চতুর্থ অবস্থা হলো প্লাজমা। এটি উচ্চ শক্তিসম্পন্ন আয়ন ও ইলেকট্রনের সমষ্টি। অত্যন্ত উচ্চ তাপমাত্রায় গ্যাস উত্তপ্ত হলে প্লাজমা তৈরি হয়। ফ্লুরোসেন্ট ল্যাম্প ও নিয়ন সাইনবোর্ডে প্লাজমা ব্যবহৃত হয়।
- বোস আইনস্টাইন কনডেনসেট (Bose Einstein Condensate): ১৯২০ সালে সত্যেন্দ্র নাথ বোস ও আলবার্ট আইনস্টাইন তত্ত্বগতভাবে এই অবস্থার ধারণা দেন। অত্যন্ত নিম্ন তাপমাত্রায় গ্যাসকে শীতল করলে এটি গঠিত হয়। এটি পদার্থের পঞ্চম অবস্থা বলে পরিচিত।
A) বিশুদ্ধ পদার্থ (Pure Substance): বিশুদ্ধ পদার্থ হলো এমন এক ধরনের পদার্থ যার গঠন নির্দিষ্ট এবং যার ধর্ম সর্বত্র একই থাকে। একে ভৌত পদ্ধতিতে অন্য পদার্থে পৃথক করা যায় না। উদাহরণ: অক্সিজেন, সোনা, জল (H₂O), লবণ (NaCl)
A1) মৌল (Element): মৌল হলো বিশুদ্ধ পদার্থের সবচেয়ে সরল রূপ, যা এক ধরনের পরমাণু দিয়ে গঠিত। সাধারণ রাসায়নিক পদ্ধতিতে একে আরও সরল পদার্থে ভাঙা যায় না। উদাহরণ: হাইড্রোজেন, কার্বন, লোহা, অক্সিজেন
(i) ধাতব পদার্থ (Metallic Substances): যেসব মৌলে ধাতুর বৈশিষ্ট্য দেখা যায়, সেগুলো ধাতব পদার্থ। এগুলো সাধারণত শক্ত, উজ্জ্বল, তাপ ও বিদ্যুতের ভালো পরিবাহী এবং পিটিয়ে পাত বা তার বানানো যায়। উদাহরণ: লোহা, তামা, সোনা, অ্যালুমিনিয়াম
প্রধান বৈশিষ্ট্য
• তাপ ও বিদ্যুতের ভালো পরিবাহী
• উজ্জ্বল পৃষ্ঠ
• পিটিয়ে পাত বানানো যায়
• তারে রূপান্তর করা যায়
• সাধারণত উচ্চ গলনাঙ্ক থাকে
(ii) উপধাতু (Metalloids): উপধাতু হলো এমন মৌল যাদের মধ্যে ধাতু ও অধাতুর উভয় বৈশিষ্ট্য থাকে। এরা বিদ্যুতের অর্ধপরিবাহী। উদাহরণ: সিলিকন, বোরন, জার্মেনিয়াম
(iii) অধাতব পদার্থ (Non-Metallic Substances): যেসব মৌলে ধাতব বৈশিষ্ট্য নেই, সেগুলো অধাতব পদার্থ। এরা সাধারণত নিস্তেজ, ভঙ্গুর (যদি কঠিন হয়), এবং তাপ ও বিদ্যুতের দুর্বল পরিবাহী।উদাহরণ: অক্সিজেন, নাইট্রোজেন, সালফার, কার্বন
প্রধান বৈশিষ্ট্য
• তাপ ও বিদ্যুতের দুর্বল পরিবাহী
• উজ্জ্বল নয়
• পিটিয়ে পাত বা তার বানানো যায় না
A2) যৌগ (Compounds): যৌগ হলো বিশুদ্ধ পদার্থ যা দুটি বা ততোধিক ভিন্ন মৌল নির্দিষ্ট অনুপাতে যুক্ত হয়ে তৈরি হয়। যৌগের ধর্ম গঠক মৌলগুলির ধর্ম থেকে সম্পূর্ণ আলাদা। উদাহরণ: জল, চিনি, লবণ, ক্লোরোফর্ম, অ্যালকোহল, ইথার।
যৌগের প্রকার
- ১. জৈব যৌগ (Organic Compounds): জীবজগত থেকে প্রাপ্ত যৌগ বা কার্বন যৌগকে জৈব যৌগ বলে। উদাহরণ: কার্বোহাইড্রেট, প্রোটিন, তেল, চর্বি।
- ২. অজৈব যৌগ (Inorganic Compounds): অজীব উৎস যেমন পাথর, খনিজ ইত্যাদি থেকে প্রাপ্ত যৌগ। উদাহরণ: সাধারণ লবণ, মার্বেল, ধোয়ার সোডা।
B) মিশ্রণ (Mixtures): দুই বা ততোধিক পদার্থ যেকোনো অনুপাতে মিশে যে পদার্থ তৈরি করে তাকে মিশ্রণ বলে। মিশ্রণে উপাদানগুলির ধর্ম অপরিবর্তিত থাকে। উদাহরণ: দুধ, সমুদ্রের জল, পেট্রোল, রং, কাঁচ, সিমেন্ট, কাঠ।
মিশ্রণের প্রকার
- ১. সমসত্ত্ব মিশ্রণ (Homogeneous Mixture): যেখানে উপাদানগুলো সমভাবে মিশে থাকে এবং আলাদা করে দেখা যায় না। উদাহরণ: লবণ জল, চিনি জল, আয়োডিন CCl₄-এ, বেনজিন টলুইন, মিথাইল অ্যালকোহল জল।
- ২. অসমসত্ত্ব মিশ্রণ (Heterogeneous Mixture): যেখানে উপাদানগুলো সমভাবে মিশে থাকে না এবং আলাদা করে দেখা যায়। উদাহরণ: বালি ও গন্ধকের মিশ্রণ, লোহার গুঁড়া ও বালির মিশ্রণ।
মিশ্রণ পৃথকীকরণ (Separation of Mixtures)
- ১. উর্ধ্বপাতন (Sublimation): S to G কঠিন থেকে সরাসরি বাষ্পে রূপান্তর। উদাহরণ: ন্যাফথালিন, আয়োডিন, অ্যামোনিয়াম ক্লোরাইড, কর্পূর। বাষ্প থেকে সরাসরি কঠিনে রূপান্তরকে Hard Frost বলে।
- ২. পরিস্রবণ (Filtration): [(S/L)+L)] to [S/L] + [L] (তরল থেকে কঠিন কণিকা ছেঁকে আলাদা করার পদ্ধতি। উদাহরণ: ইঞ্জিন তেল ছেঁকে কণা অপসারণ, চা ছেঁকে নেওয়া।
- ৩. বাষ্পীভবন (Evaporation): L TO G তরলকে বাষ্পে রূপান্তর। উদাহরণ: গ্রীষ্মে পুকুরের জল শুকানো, লবণ তৈরি।
- ৪. স্ফটিকীকরণ (Crystallization): [L] to [S] + [L] অমিশ্রিত কঠিনকে দ্রবণ থেকে স্ফটিক আকারে পৃথক করা।
- ৫. পাতন (Distillation): L to G to L তরলকে বাষ্পে রূপান্তর করে আবার তরলে পরিণত করা। উদাহরণ: তামা সালফেট ও জল, জল ও মিথাইল অ্যালকোহল আলাদা করা।
- ৬. ভগ্নাংশ পাতন (Fractional Distillation): ভিন্ন স্ফুটনাঙ্কের তরল আলাদা করা। উদাহরণ: অ্যালকোহল ও অ্যাসিটোন, পেট্রোলিয়াম থেকে বিভিন্ন জ্বালানি।
- ৭. ক্রোমাটোগ্রাফি (Chromatography): বিভিন্ন উপাদানের শোষণ ক্ষমতার পার্থক্যের উপর ভিত্তি করে পৃথকীকরণ। প্রকার: কলাম, পাতলা স্তর, কাগজ, উচ্চচাপ তরল, আয়ন-বিনিময়, গ্যাস ক্রোমাটোগ্রাফি।
উর্ধ্বপাতন (Sublimation):
উর্ধ্বপাতন হলো এমন একটি প্রক্রিয়া যেখানে কোনো কঠিন পদার্থ তরল অবস্থার মধ্য দিয়ে না গিয়ে সরাসরি বাষ্পে পরিণত হয়। এই পদ্ধতি সেইসব পদার্থ আলাদা করতে ব্যবহৃত হয় যেগুলি উর্ধ্বপাতিত হয় এবং যেগুলি হয় না। উর্ধ্বপাতিত পদার্থের উদাহরণ: ন্যাফথালিন, আয়োডিন, অ্যামোনিয়াম ক্লোরাইড, কর্পূর।
নোট: বাষ্প থেকে সরাসরি কঠিনে রূপান্তর প্রক্রিয়াকে হার্ড ফ্রস্ট বলা হয়।
পরিস্রবণ (Filtration):
এটি এমন একটি প্রক্রিয়া যেখানে কোনো তরল থেকে ভাসমান কঠিন কণাগুলিকে ফিল্টার পেপারের সাহায্যে দ্রুত ও সম্পূর্ণভাবে অপসারণ করা হয়। উদাহরণ: ইঞ্জিন তেল থেকে কঠিন কণা অপসারণ, চা তৈরির সময় পাতাগুলি ছেঁকে নেওয়া।
বাষ্পীভবন (Evaporation):
ঘরের তাপমাত্রায় তরল থেকে বাষ্পে রূপান্তর প্রক্রিয়াকে বাষ্পীভবন বলে। বাষ্পীভবনের ফলে শীতলতা সৃষ্টি হয়।
উদাহরণ: ১. গ্রীষ্মকালে পুকুর, কূপ ও হ্রদ থেকে জলের বাষ্পীভবন। ২. সমুদ্রের জল বাষ্পীভবনের মাধ্যমে সাধারণ লবণ প্রস্তুত।
গ্রীষ্মকালে মাটির কলসে রাখা জল বাষ্পীভবনের কারণে ঠান্ডা হয়ে যায়।
স্ফটিকীকরণ (Crystallization):
এই পদ্ধতি কঠিন পদার্থ পৃথক ও বিশুদ্ধ করার জন্য ব্যবহৃত হয়। এই প্রক্রিয়ায় অপবিত্র কঠিন বা মিশ্রণকে উপযুক্ত দ্রাবকের (যেমন অ্যালকোহল, জল, অ্যাসিটোন, ক্লোরোফর্ম) সাথে স্ফুটনাঙ্ক পর্যন্ত উত্তপ্ত করা হয় এবং গরম দ্রবণ ছেঁকে নেওয়া হয়। পরিষ্কার দ্রবণ ধীরে ধীরে ঠান্ডা করলে বিশুদ্ধ কঠিন স্ফটিক আকারে বেরিয়ে আসে। পরে তা ছেঁকে শুকানো হয়। জটিল মিশ্রণ পৃথক করতে ভগ্নাংশ স্ফটিকীকরণ ব্যবহার করা হয়, যেখানে উপাদানগুলি বিভিন্ন সময়ে স্ফটিক আকারে পৃথক হয়।
পাতন (Distillation):
পাতন হলো এমন প্রক্রিয়া যেখানে তরলকে উত্তপ্ত করে বাষ্পে রূপান্তরিত করা হয় এবং পরে ঠান্ডা করে সেই বাষ্পকে আবার তরলে পরিণত করা হয়। অর্থাৎ, পাতনে বাষ্পীভবন ও ঘনীভবন উভয়ই ঘটে।Distillation = Vaporisation + Condensationএই পদ্ধতি বিভিন্ন স্ফুটনাঙ্কের তরল আলাদা করতে বা দ্রবণে দ্রবীভূত অ-উদ্বায়ী কঠিন পদার্থ থেকে তরল আলাদা করতে ব্যবহৃত হয়। উদাহরণ: কপার সালফেট ও জল, অথবা জল (স্ফুটনাঙ্ক 100°C) ও মিথাইল অ্যালকোহল (স্ফুটনাঙ্ক 45°C) মিশ্রণ আলাদা করা।
ভগ্নাংশ পাতন (Fractional Distillation):
এই প্রক্রিয়া পাতনের মতোই, তবে এখানে একটি ভগ্নাংশ কলাম ব্যবহার করে দুই বা ততোধিক উদ্বায়ী তরল যাদের স্ফুটনাঙ্ক আলাদা, তাদের পৃথক করা হয়। উদাহরণ: ১. মিথাইল অ্যালকোহল ও অ্যাসিটোন পৃথক করা। ২. অপরিশোধিত পেট্রোলিয়াম থেকে পেট্রোল, ডিজেল, কেরোসিন, ভারী তেল পৃথক করা। ৩. তরল বায়ু থেকে অক্সিজেন, নাইট্রোজেন, নিষ্ক্রিয় গ্যাস ও কার্বন ডাই অক্সাইড পৃথক করা।
ক্রোমাটোগ্রাফি (Chromatography):
ক্রোমাটোগ্রাফি শব্দটি ল্যাটিন শব্দ “Chroma” থেকে এসেছে, যার অর্থ রং। এই পদ্ধতিতে মিশ্রণের উপাদানগুলির শোষণ হারের পার্থক্যের উপর ভিত্তি করে পৃথকীকরণ করা হয়।
ক্রোমাটোগ্রাফির প্রকারভেদ
(a) কলাম ক্রোমাটোগ্রাফি
(b) পাতলা স্তর ক্রোমাটোগ্রাফি
(c) কাগজ ক্রোমাটোগ্রাফি
(d) উচ্চ চাপ তরল ক্রোমাটোগ্রাফি
(e) আয়ন-বিনিময় ক্রোমাটোগ্রাফি
(f) গ্যাস ক্রোমাটোগ্রাফি
অবক্ষেপণ ও ঢালাই (Sedimentation and Decantation):
এই পদ্ধতি তখন ব্যবহৃত হয় যখন একটি উপাদান তরল এবং অন্যটি অদ্রবণীয় কঠিন, যেমন কাদা ও জল। যদি কাদাযুক্ত জলকে কিছুক্ষণ একটি বিকারে স্থিরভাবে রাখা হয়, তবে মাটি ও বালির কণাগুলি নিচে বসে যায়। এই প্রক্রিয়াকে অবক্ষেপণ বলে। উপরের পরিষ্কার তরল ধীরে অন্য বিকারে ঢেলে নেওয়া যায়। এই প্রক্রিয়াকে ঢালাই বলে।
অবস্থার পরিবর্তনের ধারণা
(a) গলনাঙ্ক (Melting Point): স্বাভাবিক চাপে কোনো কঠিন পদার্থ তাপ শোষণ করে যে স্থির তাপমাত্রায় তরলে পরিণত হয়, তাকে গলনাঙ্ক বলে। বরফের গলনাঙ্ক 0°C এবং সোডিয়াম ক্লোরাইড (NaCl)-এর গলনাঙ্ক 800°C। গলনাঙ্ক একটি নির্দিষ্ট তাপমাত্রা। তবে অপদ্রব্য থাকলে গলনাঙ্ক পরিবর্তিত হতে পারে। উদাহরণস্বরূপ, বরফ ও লবণের মিশ্রণের গলনাঙ্ক –15°C।
(b) স্ফুটনাঙ্ক (Boiling Point): স্বাভাবিক বায়ুমণ্ডলীয় চাপে তরল যে স্থির তাপমাত্রায় বাষ্পে পরিণত হয় তাকে স্ফুটনাঙ্ক বলে।
| তরল | জল | ইথানল | ক্লোরোফর্ম | অ্যাসিটোন |
|---|---|---|---|---|
| স্ফুটনাঙ্ক | 100°C | 78.3°C | 62°C | 46°C |
বায়ুচাপ কমলে স্ফুটনাঙ্ক কমে। দ্রবণীয় অপদ্রব্য স্ফুটনাঙ্ক বাড়ায়।
(c) হিমাঙ্ক (Freezing Point): যে স্থির তাপমাত্রায় কোনো তরল তাপ ত্যাগ করে কঠিনে পরিণত হয়, তাকে হিমাঙ্ক বলে। জলের হিমাঙ্ক 0°C।
(d) বাষ্পীভবন (Evaporation): ঘরের তাপমাত্রায় তরল বাষ্পে রূপান্তরিত হওয়াকে বাষ্পীভবন বলে। বাষ্পীভবনে শীতলতা সৃষ্টি হয়। উচ্চ গতিশক্তিসম্পন্ন অণুগুলি তরলের পৃষ্ঠ থেকে বেরিয়ে যায়, ফলে অবশিষ্ট অণুর গড় গতিশক্তি কমে এবং ঠান্ডা অনুভূত হয়। বাষ্পীভবন প্রভাবিত হয়
- তরলের প্রকৃতি
- তাপমাত্রা
- পৃষ্ঠের ক্ষেত্রফল
(e) বাষ্পচাপ (Vapour Pressure): নির্দিষ্ট তাপমাত্রায় তরলের সাথে সাম্যাবস্থায় থাকা বাষ্প যে চাপ প্রয়োগ করে তাকে বাষ্পচাপ বলে। এটি নির্ভর করে তরলের প্রকৃতি ও তাপমাত্রার উপর। তাপমাত্রা বাড়লে বাষ্পচাপ বাড়ে।
(f) ঘনীভবন বা তরলীকরণ (Condensation / Liquefaction): গ্যাসীয় পদার্থ নির্দিষ্ট তাপমাত্রায় ঠান্ডা হয়ে তরলে পরিণত হওয়াকে ঘনীভবন বলে। ঠান্ডা হলে গ্যাস কণাগুলি গতিশক্তি হারায় এবং কাছাকাছি এসে তরলে পরিণত হয়।
রাসায়নিক প্রতীক, সংকেত ও সমীকরণ
রাসায়নিক প্রতীক (Chemical Symbol): প্রতীক হলো কোনো মৌলের নামের সংক্ষিপ্ত রূপ। ডালটন প্রথম প্রতীক ব্যবহারের প্রচলন করেন। বার্জেলিয়াস প্রস্তাব দেন যে প্রতীক এক বা দুই অক্ষর দিয়ে হবে।
মৌলের নাম অনেক সময় স্থান বা রং থেকে এসেছে। যেমন তামার নাম এসেছে Cyprus থেকে। সোনার নাম এসেছে হলুদ অর্থবোধক শব্দ থেকে। বর্তমানে IUPAC মৌলের নাম নির্ধারণ করে।
প্রতীকের প্রথম অক্ষর বড় হাতের এবং দ্বিতীয় অক্ষর ছোট হাতের হয়। কিছু প্রতীক ল্যাটিন, জার্মান বা গ্রিক নাম থেকেও এসেছে।
১. ইংরেজি নামের প্রথম অক্ষর থেকে
- Hydrogen – H
- Carbon – C
- Oxygen – O
- Phosphorus – P
- Boron – B
- Nitrogen – N
- Fluorine – F
- Sulphur – S
২. ইংরেজি নামের দুই অক্ষর থেকে
- Helium – He
- Neon – Ne
- Nickel – Ni
- Magnesium – Mg
- Manganese – Mn
- Aluminium – Al
- Argon – Ar
- Calcium – Ca
- Chromium – Cr
- Cobalt – Co
- Chlorine – Cl
- Zinc – Zn
- Platinum – Pt
- Radium – Ra
৩. ল্যাটিন নাম থেকে
- Sodium – Natrium – Na
- Potassium – Kalium – K
- Iron – Ferrum – Fe
- Copper – Cuprum – Cu
- Silver – Argentum – Ag
- Tin – Stannum – Sn
- Gold – Aurum – Au
- Lead – Plumbum – Pb
- Mercury – Hydrargyrum – Hg
প্রথম 30 টি মৌলের তথ্য
| মৌলের নাম | প্রতীক | e/p সংখ্যা | নিউট্রন (n) | ভরসংখ্যা = p+n |
|---|---|---|---|---|
| হাইড্রোজেন | H | 1 | 0 | 1 |
| হিলিয়াম | He | 2 | 2 | 4 |
| লিথিয়াম | Li | 3 | 4 | 7 |
| বেরিলিয়াম | Be | 4 | 5 | 9 |
| বোরন | B | 5 | 6 | 11 |
| কার্বন | C | 6 | 6 | 12 |
| নাইট্রোজেন | N | 7 | 7 | 14 |
| অক্সিজেন | O | 8 | 8 | 16 |
| ফ্লোরিন | F | 9 | 10 | 19 |
| নিয়ন | Ne | 10 | 10 | 20 |
| সোডিয়াম | Na | 11 | 12 | 23 |
| ম্যাগনেশিয়াম | Mg | 12 | 12 | 24 |
| অ্যালুমিনিয়াম | Al | 13 | 14 | 27 |
| সিলিকন | Si | 14 | 14 | 28 |
| ফসফরাস | P | 15 | 16 | 31 |
| সালফার | S | 16 | 16 | 32 |
| ক্লোরিন | Cl | 17 | 18 | 35 |
| আর্গন | Ar | 18 | 22 | 40 |
| পটাসিয়াম | K | 19 | 20 | 39 |
| ক্যালসিয়াম | Ca | 20 | 20 | 40 |
| স্ক্যান্ডিয়াম | Sc | 21 | 24 | 45 |
| টাইটানিয়াম | Ti | 22 | 26 | 48 |
| ভ্যানাডিয়াম | V | 23 | 28 | 51 |
| ক্রোমিয়াম | Cr | 24 | 28 | 52 |
| ম্যাঙ্গানিজ | Mn | 25 | 30 | 55 |
| লোহা | Fe | 26 | 30 | 56 |
| কোবাল্ট | Co | 27 | 32 | 59 |
| নিকেল | Ni | 28 | 31 | 59 |
| তামা | Cu | 29 | 35 | 64 |
| দস্তা | Zn | 30 | 35 | 65 |
রাসায়নিক সংকেত (Chemical Formula): রাসায়নিক সংকেত কোনো যৌগের গঠনের প্রতীকী প্রকাশ। মৌলের সংযোজন ক্ষমতাকে যোজ্যতা বলে। যোজ্যতার সাহায্যে রাসায়নিক সংকেত লেখা হয়। উদাহরণ:
Hydrogen Chloride → HCl
Hydrogen Sulphide → H₂S
অ্যালুমিনিয়াম অক্সাইডের সংকেত
মৌল: অ্যালুমিনিয়াম – অক্সিজেন
প্রতীক : Al – O
যোজ্যতা: 3 – 2
∴ অ্যালুমিনিয়াম অক্সাইডের সংকেত = Al₂O₃
ক্যালসিয়াম অক্সাইডের সংকেত
মৌল: ক্যালসিয়াম – অক্সিজেন
প্রতীক: Ca – O
যোজ্যতা: 2 – 2
ক্যালসিয়াম অক্সাইডের সংকেত প্রথমে Ca₂O₂ হয়, সরল করলে CaO পাওয়া যায়। অতএব ক্যালসিয়াম অক্সাইডের সংকেত CaO।
রাসায়নিক সমীকরণ
রাসায়নিক সমীকরণ হলো কোনো রাসায়নিক বিক্রিয়ার প্রতীকী প্রকাশ যেখানে বিক্রিয়ায় অংশগ্রহণকারী পদার্থের প্রতীক ও সংকেত ব্যবহার করা হয়।
উদাহরণ: বাতাসে কয়লা পোড়ালে কার্বন ডাই অক্সাইড তৈরি হয়।
শব্দ সমীকরণ
কার্বন + অক্সিজেন → কার্বন ডাই অক্সাইড
রাসায়নিক সমীকরণ
C + O₂ → CO₂
রাসায়নিক সমীকরণ লেখার ধাপ
১. বিক্রিয়কের প্রতীক বা সংকেত বাম পাশে লিখতে হয় এবং তাদের মাঝে (+) চিহ্ন দিতে হয়।
২. উৎপন্ন পদার্থের সংকেত ডান পাশে লিখতে হয়।
৩. মাঝখানে তীর চিহ্ন (→) দিতে হয়।
৪. পদার্থের অবস্থা বোঝাতে (g), (l), (aq), (s) ব্যবহার করা হয়।
ম্যাগনেশিয়াম ফিতা জ্বললে সাদা গুঁড়ো ম্যাগনেশিয়াম অক্সাইড তৈরি হয়।
Mg (s) + O₂ (g) → MgO (s)
বিষমগন্ধতা (Rancidity): যখন খাদ্যের গন্ধ, স্বাদ ও রং পরিবর্তিত হয় তখন তাকে বিষমগন্ধতা বলে। চর্বি ও তেল জারণ হলে এ অবস্থা সৃষ্টি হয়। তাই অ্যান্টিঅক্সিডেন্ট ব্যবহার করা হয়। বাতাসরোধী পাত্রে রাখলে জারণ ধীর হয়।
ক্ষয় (Corrosion): ধাতু আর্দ্রতা বা অ্যাসিডের সংস্পর্শে এলে ক্ষয়প্রাপ্ত হয়। রূপার কালো স্তর ও তামার সবুজ স্তর ক্ষয়ের উদাহরণ। লোহা মরিচা ধরে লালচে বাদামী স্তর তৈরি করে। মরিচা হলো hydrated ferric oxide (Fe₂O₃·xH₂O)।